EUROPSKI TJEDAN PREVENCIJE RAKA VRATA MATERNICE 2023.
Europski tjedan prevencije raka vrata maternice obilježava se svake godine u trećem tjednu mjeseca siječnja, na inicijativu Europske asocijacije protiv raka maternice, a kako bi se u općoj populaciji podigla svijest o toj bolesti, o mogućnostima prevencije i ranog otkrivanja.
Svjetska zdravstvena organizacija 2020. godine je pokrenula globalnu inicijativu kako bi se ubrzala eliminacija karcinoma vrata maternice do 2030. godine implementacijom triju interventnih mjera:
- cijepljenje barem 90% djevojaka u dobi do 15 godina s HPV cjepivom,
- primarni probir barem 70% žena u dobi do 35 godina s HPV testom, i još jednom u dobi do 45 godina,
- učinkovito liječenje barem 90% svih otkrivenih premalignih lezija i invazivnih karcinoma.
U Hrvatskoj se već više od 5o godina provodi oportunistički probir raka vrata maternice citološkim PAPA testom, a 2012. godine je započeo nacionalni program organiziranog probira uz pozivanje žena u dobi od 25 do 64 godine, a koje nisu u prethodne tri godine obavile PAPA test. Program je 2016 godine obustavljen zbog planiranih tehničkih poboljšanja.
Svjetska zdravstvena organizacija preporuča HPV test kao test izbora za probir, međutim njegova implementacija nailazi na brojne barijere diljem svijeta zbog niza čimbenika, od nedostatka potrebne tehničke infrastrukture i nedostupnosti validiranih testova pa do postojeće zakonske regulative i infrastrukture temeljene na citološkom probiru. Ono što je sigurno, a to je nužnost revidiranja postojećih preporuka i smjernica koje u Republici Hrvatskoj datiraju još iz 2012. godine od kada je došlo do značajnog napretka u mikrobiološkoj molekularnoj dijagnostici.
- HPV JE NAJČEŠĆA SPOLNO PRENOSIVA INFEKCIJA.
- VEĆINA TIH INFEKCIJA, GOTOVO 90% NJIH PROLAZI UNUTAR DVIJE GODINE SAMOIZLJEČENJEM.
- RAK VRATA MATERNICE POSLJEDICA JE PERZISTENTNE, TRAJNE INFEKCIJE POJEDINIM TIPOVIMA HUMANOG PAPILOMA VIRUSA KOJI SE NAZIVAJU VISOKORIZIČNIM
- 14 JE KLINIČKI NAJZNAČAJNIJIH VISOKORIZIČNIH TIPOVA HUMANOG PAPILOMA VIRUSIMA
- 70% SVIH KARCINOMA VRATA MATERNICE UZROKUJU TIPOVI 16 i 18.
Rak vrata maternice je lakše spriječiti nego liječiti!
Nacionalni preventivni program ranog otkrivanja raka vrata maternice (hzjz.hr)

ZAŠTO ODABRATI HPV TEST KAO TEST PROBIRA?
Probir temeljen na HPV testiranju pokazao se učinkovitijim u odnosu na probir temeljen na citomorfologiji u postizanju smanjenja incidencije i smrtnosti od raka vrata maternice. Sve veći broj zemalja odabire HPV test za primarni test probira karcinoma vrata maternice. Osnovni cilj probira je pravovremeno otkrivanje prekanceroznih lezija na vratu maternice, time povećanog rizika za nastanak karcinoma.
Iako danas na tržištu postoji više od 250 dostupnih različitih testova:
- SAMO JE 5 TESTOVA DOBILO ODOBRENJE OD FDA ( Američka agencija za hranu i lijekove ) ZA PROBIR RAKA VRATA MATERNICE U KOTESTIRANJU SA CITOLOGIJOM
- SAMO 3 TESTA IMAJU ODOBRENJE DA SE KORISTE KAO PRIMARNI TEST PROBIRA
KLJUČNO JE ODABRATI PRIKLADAN HPV TEST
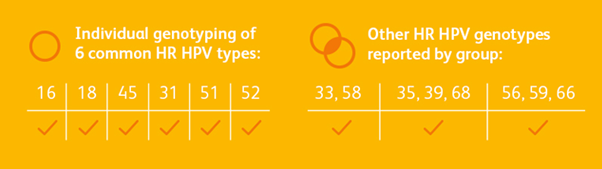
Služba za mikrobiologiju i parazitologiju ZJZ Zadar za određivanje DNA visokorizičnih genotipova HPV koristi jedan od tri FDA odobrena testa – BD OnclarityTM HPV Assay koji omogućuje PROŠIRENO GENOTIPIZIRANJE.
Genotipovi 16, 18 i 45 su zajedno odgovorni za najmanje 75% karcinoma pločastih stanica i 94% adenokarcinoma.
Učestalost genotipova 16 i 18 pada kako raste stopa procijepljenosti protiv HPV.
Genotipovi 18 i 45 značajno se češće identificiraju kao uzročnici adenokarcinoma.
Genotipovi 31,33,58 imaju podjednak rizik za razvoj CIN3+ kao i genotip 18.
Genotip 31 je drugi najčešći visokorizični HPV tip za razvoj CIN3+.
BD Onclarity TM HPV Assay omogućuje pojedinačno izvještavanje rezultata za 6 visokorizičnih genotipova i grupne rezultate za preostalih 8 genotipova.
Na taj način omogućuje individualnu procjenu rizika za razvoj premalignih i malignih lezija a time strategiju daljnjeg praćenja pacijenata.
1. Stoler MH et al. Gynecol Oncol. 2019;153(1):26–33. 2. Bonde J et al. Int J Cancer. 2019; doi:10.1002/ijc.32291. 3.Elfgren K et al. Am J Obstet Gynecol. 2017;216(3):264.e1–264.e7. 4. Radley D et al. Hum Vaccin Immunother. 2016;12(3):768–772. 5. Bottari F et al. J Low Genit Tract Dis. 2019;23(1):39–42. 6. World Health Organization, Department of Reproductive Health and Research. Cervical cancer, human papillomavirus (HPV), and HPV vaccines—key points for policy-makers and health professionals. 2007. 7. Oliver SE et al. J Infect Dis. 2017;216(5):594–603. 8. Drolet M et al. Lancet Infect Dis. 2015;15(5):565–580. 9. Garland SM et al. Clin Infect Dis. 2016;63(4):519–527. 10. Schiffman M et al. Gynecol Oncol. 2015;138(3):573–578. 11. Schiffman M et al. Int J Cancer. 2016;139(11):2606–2615. 12. BD Onclarity™ HPV Assay EU Package Insert (8089899). 13. Tjalma WAA et al. Eur J Obstet Gynecol Reprod Biol. 2013;170(1):45–46.
Autor: Ivanka Matas, dr. med. spec. mikrobiologije - voditeljica Službe za mikrobiologiju i parazitologiju Zavoda za javno zdravstvo Zadar


